2020进口保健食品备案全景透视 日本、德国、丹麦首备成功背后的市场机遇与合规逻辑
2020年,中国进口保健食品备案工作继续稳步推进,市场准入与监管体系日益成熟。其中,日本、德国、丹麦等国家在特定产品类别上实现“首备成功”,成为行业关注的焦点。这不仅标志着相关产品正式获得进入中国市场的“通行证”,也折射出全球保健食品产业格局的演变与中国消费者需求偏好的变迁。对相关备案信息进行系统梳理与深度分析,对把握行业趋势、理解监管导向具有重要意义。
一、2020年进口保健食品备案总体态势
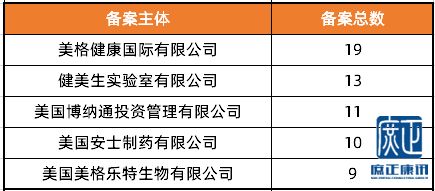
根据国家市场监督管理总局(SAMR)及相关数据库公开信息,2020年进口保健食品备案数量保持稳定增长。备案产品仍集中于营养素补充剂(如维生素、矿物质)等法规相对清晰、原料目录明确的类别。备案主体以在华注册的境外生产商或其境内责任单位为主,显示出品牌方对中国市场长期投入的决心。监管层面,延续了“备案制”与“注册制”双轨并行模式,对使用《保健食品原料目录》及《允许保健食品声称的保健功能目录》内成分与功能的产品实施备案管理,流程效率较高。
二、日本、德国、丹麦“首备成功”案例解析
1. 日本:精细化营养与原料优势的体现
2020年,日本某知名品牌以“胶原蛋白肽”为主要成分的饮品成功完成备案。这并非新原料,但日本企业在产品配方精细化、口味剂型创新及品质控制方面表现突出。该备案成功,体现了中国市场对具有美容、关节健康等宣称的特定功能产品,以及日本在海洋生物提取物、发酵技术等领域原料口碑的认可。日本保健食品素以“精细”、“温和”、“剂型多样”著称,其备案策略往往聚焦于其优势原料(如肽类、特定植物提取物)与差异化的产品形态。
2. 德国:科学背书与“品质可靠”标签的强化
德国成功备案的产品中,以复合维生素矿物质片剂、Omega-3脂肪酸类产品为代表。德国保健食品工业与药学传统结合紧密,强调科学实证与生产质量管理。其“首备成功”的产品,往往附有严谨的科学研究支持,生产工艺符合欧盟及国际高标准。这精准对接了中国中高端消费群体对“德国品质”的信赖,尤其是在母婴营养、基础营养补充等领域。德国产品的成功备案,强化了其在华“科学、严谨、可靠”的品牌形象,为后续同类产品进入铺平了道路。
3. 丹麦:益生菌领域的领先地位与市场先机
丹麦在益生菌及相关制品领域的备案取得突破,具有标志性意义。依托全球领先的菌种研发与生产企业,丹麦备案的特定菌株益生菌产品成功进入目录并完成备案。这得益于中国对益生菌类保健食品的法规路径逐渐明晰,以及市场对肠道健康、免疫支持等功能需求的激增。丹麦“首备成功”,不仅巩固了其在全球益生菌供应链中的核心地位,也抓住了中国消费者健康意识提升带来的早期市场红利。
三、备案信息背后的行业趋势与挑战分析
趋势洞察:
1. 来源地多元化与优势细分:备案成功的国家不再局限于传统的美澳大国,日、德、丹等国的成功,显示出市场正根据各国产业特长进行细分领域的深耕。
2. 功能诉求精准化:备案产品功能集中指向美容(抗衰老)、关节健康、肠道健康、基础营养补充等,与都市人群的健康痛点高度契合。
3. “科学证据”与“原料溯源”成为关键:无论是德国的科研背书,还是丹麦的菌株专利,抑或日本的原料工艺,提供可信的科学依据和透明的原料信息,是赢得监管与消费者双重信任的核心。
挑战提示:
1. 法规适应性:各国产品配方习惯与中国的《原料目录》、《备案细则》需要精准对接,任何成分、用量、声称的偏差都可能导致备案失败。
2. 市场同质化竞争:基础营养素补充剂等备案类别进入门槛相对较低,市场竞争激烈,“首备”带来的窗口期红利可能缩短。
3. 消费者教育成本:新产品、新功能需要大量的市场教育,备案成功仅是第一步,品牌建设与渠道拓展同样至关重要。
四、结论与展望
2020年日本、德国、丹麦等国在进口保健食品备案上取得的成功,是各国产业优势与中国市场法规、消费者需求成功对接的缩影。它预示着中国进口保健食品市场正朝着来源地更多元、产品更细分、科技含量更高的方向发展。对于行业参与者而言,深入分析备案数据,洞察监管风向,结合自身优势选择精准的品类与功能赛道,并构建从原料到声称的完整科学证据链,是在这一市场赢得长期发展的必由之路。随着备案目录的动态调整与扩充,以及跨境电子商务等新渠道的融合,进口保健食品市场的信息处理与分析将变得更加重要,成为企业战略决策不可或缺的一环。
如若转载,请注明出处:http://www.ecatch-edc.com/product/31.html
更新时间:2026-06-05 14:09:34